원자 집합 해 분자를 만듭니다.
분자와 분자간에는 “분자간 력 ‘이라는 힘이 작용 고체화 (결정화)합니다.
화학 결합은 원자가 안정을 추구 閉殻 구조를 획득하게 반응이며, 이러한 이유로 원자는 분자와 결정 등을 만들어 존재하고있는 것입니다.
수지는 주로 다음과 같은 4 개의 결합이 있습니다.
1.공유 결합
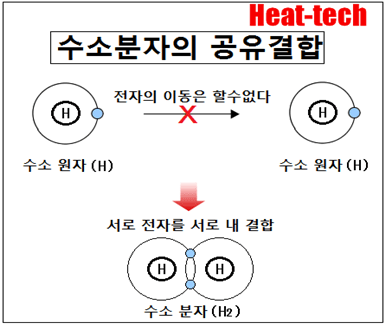
공유 결합은 원자들은 서로 전자를 공유함으로써 생기는 화학 결합입니다. 결합은 매우 강하고 분자는 공유 결합에 의해 형성됩니다 (단 원자 분자는 제외). 또한 공유 결합에 의해 형성되는 결정이 공유 결합 결정합니다. 배위 결합을 공유 결합의 일종입니다.
2.이온 결합
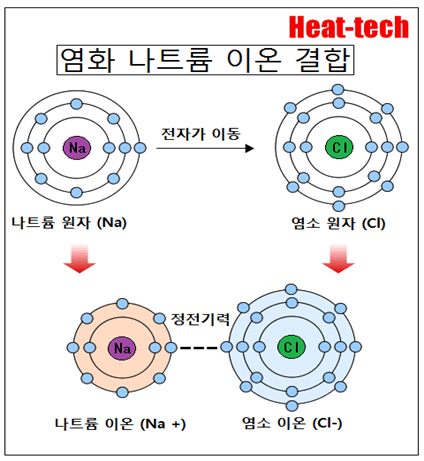
이온 결합은 양전하를 갖는 양이온 (양이온)와 음전하를 갖는 음이온 (음이온) 사이의 정전 인력에 의한 화학 결합입니다.
이 결합해서 이온 결정이 형성됩니다.
공유 결합과 대비되어 연결성 궤도가 전기 음성도가 높은 쪽의 원자로 지방화 한 극한으로 해석 할 수 있습니다.
3.수소결합
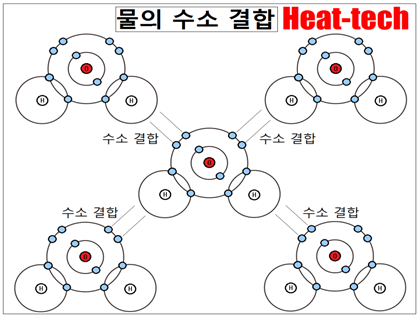
수소결합(水素結合)은 전기 음성도가 큰 원자(음성원자陰性原子)에 공유결합에서 결부된 수소원자가, 근방에 위치한 N질소, O산소, S유황, F불소, π전자계등의 고립 전자대와 만드는 비공유결합성의 인력적 상호작용입니다.
수소결합에는, 다른 분자의 사이에 작용하는 물건(분자간력)과 단일인 분자의 다른 부위의 사이(분자내)에 일하는 것이 있습니다.
전기적으로 약한 양성 (δ +)를 띤 수소 (위 그림 : 물 분자의 예) 주변의 전기 음성 원자 사이에 일으키는 정전기적인 힘으로 설명됩니다.
즉, 쌍극자 상호 작용 가운데 특별 강한 것,라고 생각할 수도 있습니다.
단 수소결합은 이온 결합과 같은 무지향성의 상호작용이 아니고, 수소·비공유 전자대의 상대배치에도 의존하는 상호작용이기 때문, 수소 이온(프로톤(proton))의 「공던지기」라고 표현될 것도 있습니다.
수소결합은 물 등의 무기물에 있어서도, DNA등의 유기물에 있어서도 일합니다.
수소결합은 물의 성질, 예를 들면 상 변화 등의 열적성질,혹은 물과 다른 물질과의 친화성등에 있어서 중요한 역할을 짊어지고 있습니다.
수소결합을하는 물질은 물에 잘 녹아 있습니다.물과 수소결합을하여 용매와 용질 사이의 인력이 강하게되기 때문입니다.
4.반 데르 워스 결합 (Van der Waals bond)
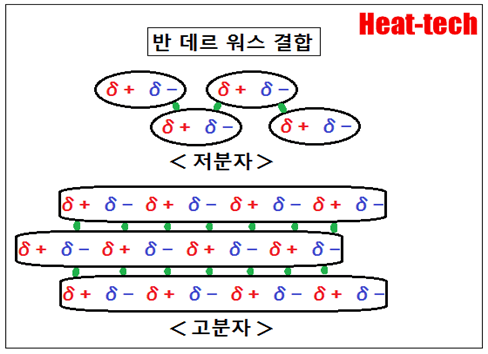
분자는 전기적으로 중성 전반적으로 전하를 가지고 있지 않기 때문에, 양이온과 음이온 사이에서 일하는 같은 강한 쿨롱 힘이 분자간에 작용하는 것은 아닙니다.
그러나 분자는 마이크로 보면 원자핵과 그 주위를 돌아 다니는 전자의 집합체이기 때문에, 분자 내에서 순간적으로 전자가 불균등하게 분포 할 수 있으며, 따라서 분자 내에 δ +와 δ-의 부분 전하가 발생합니다.
이 임시 극화 한 분자는 인접한 분자를 일시적으로 분극시켜 분자끼리 서로 약하고 당기는 것입니다.
분자간의 이러한 상호작용을 판데루와스 힘 (Van der Waals force)이라고 말합니다.
이 판데루와스 힘의 결부를 판데루와스 결합 이라고 합니다.
분자간력에 의한 일시적인 정전상호작용(静電相互作用)은 이온 결합에 의한 것에 비교해서 1/10∼1/1000의 강도밖에 없습니다.
그러나, 고분자의 비이온성의 원자의 수는 방대하므로, 분자간력에 근거하는 화학결합도 쌓아 올릴 수 있으면 결합력으로서 상당한 영향력을 가집니다.
즉 분자를 계류하는 분자 내 결합을 제외하고 분자간 힘은 물질을 구성하는 분자를 결합하는 힘을 제공하고 물체의 모양이나 특성을 표현하고 있습니다.
5.공유 결합의 결합 에너지
| I – I | 151 kJ/mol |
| F – F | 159 kJ/mol |
| Br – Br | 192 kJ/mol |
| Cl – Cl | 247 kJ/mol |
| H – H | 435kJ/mol |
| O = O | 498 kJ/mol |
| HO – H | 499 kJ/mol |
| CH3 – H | 439 kJ/mol |
| CH3 – CH3 | 385 kJ/mol |
| CH2 = CH2 | 682 kJ/mol |
| N ≡ N | 945 kJ/mol |
기호의 의미 – : 단일 결합 = : 이중 결합 ≡ : 삼중 결합
6. 분자간 력의 힘
| 분자 내 결합 | 분자간 결합 | 결합 강도 비 | |
|---|---|---|---|
| 공유 결합 | ○ | × | 강대 |
| 이온 결합 | ○ | ○ | 1000 |
| 수소 결합 | ○ | ○ | 100 |
| 반 데르 워스 결합 | × | ○ | 1 |
* 반 데르 워스 결합은 분자 단위의 수치입니다. 분자 수가 수십만 단위가되는 고분자 수지로는 매우 강력합니다.
모노머의 중합 수축
| 수지 이름 | 중합 수축률 % |
|---|---|
| 에틸렌 | 66.0 |
| 염화 비닐 | 34.4 |
| 아쿠리로니토루 | 31.0 |
| 에틸렌 옥사이드 | 23.0 |
| 메틸 메타 크릴 레이트 | 21.2 |
| 비닐 아세테이트 | 20.9 |
| 디 알릴 부마 속도 | 17.2 |
| n- 프로필 메타 크릴 레이트 | 15.0 |
| 스티렌 | 14.5 |
| 디 에틸렌 글리콜 비스 알칼리 카보네이트 | 14.0 |
| 에피 클로로 히 드린 | 12.0 |
| 디 알릴 프탈레이트 | 11.8 |
| N- 비닐 카바 졸 | 7.5 |
 HEAT-TECH 최선의 기술 온라인(on-line) 샵
HEAT-TECH 최선의 기술 온라인(on-line) 샵